Ciencias de los Alimentos/ Food Sciencies
Cienc Tecn UTEQ (2019) 12(1) p 31-42 ISSN 1390-4051; e-ISSN 1390-4043
Microbiota intestinal humana y dieta
Human gut microbiota and diet
Carlos Alberto Padrón Pereira
Asociación RVCTA. Avenida Andrés Bello Nº 101-79, Sector La Pastora, Municipio Valencia, Estado Carabobo, C. P. 2001,
República Bolivariana de Venezuela. carlospadron1@gmail.com
Rec.: 18.01.2018. Acept.: 06.06.2019.
Publicado el 30 de julio de 2019
Resumen
Abstract
a dieta es un factor que impulsa la composición y
iet is a factor driving the composition and
L
el metabolismo de la microbiota intestinal (M-I),
D
metabolism of the gut microbiota, and
y los macronutrientes ejercen un gran impacto en la
macronutrients have a great impact on microbiota.
(M-I). Los carbohidratos no digeribles pueden producir
Dietary non-digestible carbohydrate can produce
marcados cambios en la (M-I), las fibras dietéticas son
marked changes in the gut microbiota, dietary fibers
los principales impulsores de la composición y función
are major drivers of gut microbiota composition and
de la (M-I), permiten estimular el predominio de una
function, stimulating the dominance of bacteria able
(M-I) capaz de utilizar estos sustratos como fuente de
to utilize these substrates as energy source, but these
energía, pero estos efectos dependen tanto del tipo de
effects depend on both the type of fiber and the initial
fibra como de la composición inicial de la (M-I) de
composition of an individual’s gut microbiota. Protein
un individuo. El metabolismo proteico por la (M-I) da
metabolism by gut microbiota results in additional
como resultado productos adicionales, algunos de los
products, some of which are potentially harmful to host
cuales son potencialmente dañinos para la salud del
health. Firmicutes, Bacteroidetes and Actinobacteria
huésped. Firmicutes, Bacteroidetes y Actinobacteria
are the three major phyla that inhabit the human large
son los tres filos principales que habitan en el intestino
intestine. The genera Bacteroides is associated with
grueso humano. El género Bacteroides se asocia con
meat-based diets, the families Ruminococcaceae
dietas basadas en carne, las familias Ruminococcaceae
and Lachnospiraceae are associated with diets rich
y Lachnospiraceae con dietas ricas en polisacáridos
in complex plant polysaccharides, and the genera
complejos de plantas y el género Prevotella con dietas
Prevotella is associated with diets high in sugar but
altas en azúcar pero bajas en grasas y proteínas. La
low in fat and protein. Diet can be used to modulate
dieta puede usarse para modular la composición y
the composition and metabolism of the gut microbiota.
el metabolismo de la (M-I). Una estrategia dietética
One dietary strategy for modulating the microbiota is
para modular (M-I) es el consumo de fibra dietética y
consumption of dietary fiber and prebiotics. This review
prebióticos. Esta revisión tiene como objetivo describir
aims at describing knowledge about gut microbiota,
conocimiento sobre la (M-I), orientado hacia un uso de
oriented towards a use of diet to provide benefits to
la dieta para proporcionar beneficios a la salud humana..
human health.
Palabras clave: alimentos saludables, bacterias
Key words: healthy foods, gut bacteria, microbial
intestinales, diversidad microbiana, fibras dietéticas,
diversity, dietary fibers, dietary patterns, health.
patrones dietéticos, salud.
31
Padrón, 2019
las superficies del cuerpo humano que están expuestas
al entorno externo; incluye la piel, la cavidad oral, el
Introducción
tracto respiratorio, urogenital y el gastrointestinal. El
tracto gastrointestinal es el más densamente colonizado
a microbiota intestinal humana está influenciada
y la compleja comunidad de microorganismos que allí
L
por varios factores (Graf et al., 2015). La dieta y
reside o pasa a través de ella se conoce como microbiota
el estilo de vida moderna, entre otros, ha contribuido
intestinal (Gerritsen et al., 2011).
a generar un cambio en los patrones de colonización
En el vocabulario utilizado para describir
microbianos alterando la composición de la microbiota.
las comunidades microbianas, la palabra microbiota
La dieta es considerada como uno de los principales
representa un conjunto de microorganismos que
impulsores en la conformación de la microbiota
reside en un entorno previamente establecido, como el
intestinal a lo largo de la vida (Thursby y Juge, 2017).
intestino humano; y el microbioma comprende todo el
La relación existente entre la microbiota intestinal, la
material genético dentro de una microbiota.
salud y la enfermedad, al mismo tiempo se relaciona
Las bacterias que viven en nuestros intestinos,
con diferentes patrones alimentarios, entre ellos los
antes “flora intestinal” o “microflora intestinal”, ahora
caracterizados por abundancia de cereales, tubérculos,
“microbiota intestinal”, se desarrollan posterior al
frutas y otros vegetales, y los que se basan en un consumo
nacimiento ya que nacemos estériles. En un bebé
de alimentos refinados, carnes y otros productos de
amamantado la microbiota será principalmente
origen animal.
bifidobacterias y será diferente a la de un bebé
Como las bacterias se especializan en la
alimentado con fórmulas para lactantes. Al transcurrir
fermentación de diferentes sustratos, las dietas pueden
el tiempo la microbiota es influenciada por la dieta, el
proporcionar una gama de factores promotores del
entorno, el uso de antibióticos. Como adultos jóvenes,
crecimiento y de inhibición del crecimiento para
nuestra microbiota intestinal contiene
100 billones
filotipos específicos
(Flint et al.,
2012; Graf et al.,
de microorganismos, incluyendo como mínimo 1000
2015). La interacción entre componentes de la dieta y la
especies diferentes de bacterias. Solo 1/3 es común en
microbiota intestinal podría ser, en parte, responsable de
todas las personas y los otros 2/3 son específicos de
sus beneficios para la salud (Etxeberria et al., 2016).
cada persona. Con el paso de los años, como personas
Por evidencias de que alteraciones dietéticas
mayores, la microbiota será diferente a la de adultos
producen cambios en la microbiota intestinal, existe un
jóvenes. No obstante, de acuerdo con Bian et al.
marcado interés sobre el papel de los microorganismos
(2017), en el caso de personas mayores saludables, la
en la fisiología humana y diversas estrategias se han
microbiota puede ser similar a la de adultos jóvenes
desarrollado para intentar corregir trastornos modulando
saludables. El ecosistema microbiano que se encuentra
la composición de la microbiota intestinal.
en personas extremadamente ancianas, está enriquecido
La literatura sobre estudios experimentales
en Akkermansia, Bifidobacterium y la familia
y clínicos orientados a describir los efectos de la
Christensenellaceae, asociadas a la salud (Biagi et al.,
microbiota en respuestas fisiológicas de los huéspedes
2016). Existe relación entre la dieta, la microbiota y el
es abundante y los descubrimientos están abriendo
estado de salud, e indica un papel para las alteraciones
nuevos caminos en la comprensión de diversas
de la microbiota impulsadas por la dieta en diferentes
enfermedades inflamatorias y metabólicas, entre otras.
tasas de deterioro de la salud con el envejecimiento
Preponderantemente se ha manifestado en la literatura
(Claesson et al., 2012).
el interés sobre cómo la dieta influye en la composición
La microbiota intestinal desempeña un papel
y funcionalidad de la microbiota intestinal.
en los procesos metabólicos, nutricionales, fisiológicos
Para la revisión se consultó literatura
e inmunológicos en el cuerpo humano. Participa en
disponible en bases de datos, complementariamente,
la defensa contra patógenos por mecanismos como
con opciones de búsqueda de artículos publicados por
la resistencia a la colonización y la producción de
editoriales; PubMed, Nature Research/Springer Nature,
compuestos antimicrobianos. Además, la microbiota
British Journal of Nutrition, Science/AAAS, entre otras.
intestinal participa en el desarrollo, la maduración y el
El objetivo de esta revisión es resumir parte de
mantenimiento de las funciones sensoriales y motrices
la evidencia de estudios en humanos publicados sobre
gastrointestinales, la barrera intestinal y el sistema
el papel de la dieta en la composición de la microbiota
inmune de la mucosa (Gerritsen et al., 2011).
intestinal, orientados hacia la salud humana.
La microbiota puede adaptar su composición a
la dieta, p. ej., japoneses pueden digerir algas marinas
Microbiota intestinal y dieta
de su dieta diaria gracias a enzimas que su microbiota ha
Los microorganismos colonizan prácticamente todas
adquirido de bacterias marinas (Hehemann et al., 2010;
32
Ciencia y Tecnología. 2019. 12(1):31-42
Microbiota intestinal humana y dieta
se pueden clasificar como prebióticas; sin embargo, la
mayoría de los prebióticos se pueden clasificar como
fibras dietéticas (Slavin, 2013). Un panel de expertos en
microbiología, nutrición e investigación clínica actualizó
la definición de prebiótico: “un sustrato que es utilizado
selectivamente por microorganismos huéspedes que
confieren un beneficio para la salud”. Mientras que los
probióticos son microorganismos vivos que benefician
la salud del huésped, los prebióticos no, sino sustratos
que sirven como nutrientes para los microorganismos
beneficiosos albergados por el huésped
(Gibson et
al.,
2017). La introducción de probióticos (especies
bacterianas “benéficas” como Bifidobacterium bifidum)
o la adición de prebióticos (como fructooligosacáridos)
que promueven el crecimiento y la actividad de ciertas
especies bacterianas son los métodos convencionales
para manipular la comunidad microbiana intestinal.
Los avances en la secuenciación de alto rendimiento
y la metabolómica han llevado a la aparición de
posbióticos que se pueden utilizar para manipular
Figura
1. Disbiosis de la microbiota intestinal
directa y específicamente la función de la microbiota
manifestada como aumento de bacterias causantes
de enfermedades
(Klemashevich et al.,
2014). Los posbióticos son
productos finales metabólicos de las bacterias, entre
Nishijima et al., 2016). La microbiota puede adaptarse,
ellos el butirato, que se produce a partir de fibra
no obstante, también puede ocurrir una pérdida de
dietética, y cuando está presente en cantidad suficiente,
balance en su composición que tiene relación con el
se convierte en la principal fuente de energía para
equilibrio entre las bacterias beneficiosas (salud) y las
células epiteliales colónicas; por otro lado el propionato,
patógenas (enfermedad) en la microbiota, una alteración
que se transfiere al hígado donde sirve como precursor
conocida como disbiosis intestinal, y esto, genera
de la gluconeogénesis hepática (Schnorr et al., 2014) y
problemas de salud de todo tipo. En el mismo sentido,
el acetato, que cumple un papel en la capacidad de las
la disbiosis puede manifestarse como el aumento de
bifidobacterias para inhibir enteropatógenos (Fukuda
las bacterias causantes de enfermedades (Figura 1), la
et al., 2011). El butirato, propionato y acetato, que son
disminución de especies bacterianas beneficiosas para
ácidos grasos de cadena corta, productos principales de
la salud y/o la reducción de la diversidad de especies
la fermentación de la fibra dietética en el intestino grueso,
bacterianas. Los problemas de salud son innumerables
desempeñan un papel importante en el mantenimiento
y entre las opciones para restablecer el balance se
de la función de la barrera intestinal (Kiefer et al.,
encuentran: una buena nutrición, los probióticos,
2006; Chen et al., 2017); fundamentales en aspectos
prebióticos y posbióticos.
fisiológicos del hospedador, tales como, la adquisición
Los probióticos son microorganismos vivos
de nutrientes, la función inmune, la señalización celular,
(en la mayoría de los casos, bacterias) que son similares
el control de la proliferación y protección de patógenos
a los microorganismos beneficiosos que se encuentran
(Schnorr et al., 2014).
en el intestino humano. También se les llama “bacterias
La mayor parte de la microbiota intestinal reside en el
amigas” o “buenas bacterias”. Los probióticos están
intestino grueso; ubicación principal de la fermentación
disponibles para los consumidores principalmente
bacteriana (Korpela, 2018).
en forma de suplementos dietéticos y alimentos
Las especies bacterianas dominantes en el tracto
(NCCIH, 2018). La actual definición de probióticos es:
gastrointestinal humano se dividen en
3 filos: el
“microorganismos vivos que, cuando se administran en
filo Firmicutes
(p. ej., Ruminococcus, Clostridium,
cantidades adecuadas, confieren un beneficio para la
Eubacteria), el filo Bacteroidetes (p. ej., Porphyromonas,
salud del huésped” (Hill et al., 2014). Los prebióticos
Prevotella) y el filo Actinobacteria (Bifidobacterium)
son ingredientes alimentarios no digeribles que
(Rajoka et al.,
2017); Proteobacteria, Fusobacteria,
estimulan el crecimiento de bacterias bifidogénicas y
Cianobacteria y Verrucomicrobia suelen estar menos
ácido lácticas en el tracto gastrointestinal. Típicamente,
representados
(D’Argenio y Salvatore,
2015). El
los prebióticos consisten en fibras dietéticas y
único representante conocido del filo Verrucomicrobia
oligosacáridos (Patel y Goyal, 2012). No todas las fibras
es Akkermansia muciniphila
(Hugon y Salvatore,
Ciencia y Tecnología. 2019. 12(1):31-42
33
Padrón, 2019
Figura 2. Composición de la microbiota intestinal. Modificado de Rajoka et al. (2017) y con información de
Hugon y Salvatore (2015).
2015). Otras bacterias, tales como Lactobacillus,
caracterizó por una relativamente mayor abundancia
Streptococcus y Escherichia coli (Enterobacteriaceae)
de Bacteroidetes y menor de Firmicutes. Hadza mostró
se encuentran en menor cantidad. Con base en la
mayor enriquecimiento en los filos Proteobacteria y
evidencia de las tecnologías genómicas, se encontró que
Spirochaetes, que fueron extremadamente raros en la
los filos Firmicutes y Bacteroidetes son las poblaciones
microbiota italiana, mientras que el filo Actinobacteria,
bacterianas dominantes en el tracto gastrointestinal
una componente subdominante importante de la
(Figura 2) (Rajoka et al., 2017).
microbiota italiana, estuvo casi completamente
La microbiota se agrupa de acuerdo con patrones de
ausente en la microbiota Hadza. A nivel de género, la
dietas basadas en plantas o en animales. La diversidad
microbiota intestinal Hadza estuvo comparativamente
bacteriana en mamíferos es más alta entre los herbívoros,
enriquecida en Prevotella, Eubacterium, Oscillibacter,
seguidos de omnívoros y luego carnívoros (Ley et al.,
Butyricicoccus,
Sporobacter,
Succinivibrio,
2008), además, composicional y funcionalmente distinta
Treponema y agotada en Bifidobacterium, Bacteroides,
(Muegge et al., 2011).
Blautia, Dorea, Lachnospiraceae no clasificada,
Schnorr et al. (2014) caracterizaron la microbiota
Roseburia, Faecalibacterium, Ruminococcus y
intestinal de los Hadza en Tanzania
(cazadores-
Erysipelotrichaceae no clasificada. Además de muchos
recolectores) en comparación con la de italianos en
géneros no clasificados pertenecientes a Bacteroidetes,
Bolonia. La dieta Hadza consiste en alimentos silvestres
el orden Clostridiales y la familia Ruminococcaceae.
que se dividen en 5 categorías principales: carne, miel,
Una variedad de fibras dietéticas (p. ej., celulosa,
baobab, bayas y tubérculos. No practican ningún cultivo
hemicelulosas, pectinas, gomas, fructanos) y almidones
o domesticación de plantas y animales, y reciben un
resistentes en la dieta, que contienen una gama de
mínimo de cantidades de productos agrícolas de fuentes
unidades de monosacáridos y enlaces α y β, es más
externas. En comparación, la dieta italiana es casi en su
compatible con una variada comunidad microbiana
totalidad productos agrícolas comerciales y se adhiere en
gastrointestinal en comparación con una dieta que
gran medida a la dieta mediterránea: abundantes plantas,
tiene una carga de sustrato menos diversa (p. ej., dietas
fruta fresca, pasta, pan y aceite de oliva; cantidades
refinadas) (Holscher, 2017).
bajas a moderadas de productos lácteos, aves de corral,
De Filippo et al.
(2010) caracterizaron la
pescado y carne roja; la mayoría de los carbohidratos
microbiota fecal de niños sanos del grupo étnico
basados en almidón fácilmente digerible, azúcar y muy
Mossi en Burkina Faso en comparación con la de
poca fibra soluble o insoluble. Firmicutes y Bacteroidetes
niños sanos del área urbana de Florencia en Italia. La
fueron los filos dominantes en la microbiota intestinal
dieta de los niños Mossi es baja en grasas y proteínas
tanto en los Hadza como en los italianos; Hadza se
animales, rica en almidón, fibra y polisacáridos
34
Ciencia y Tecnología. 2019. 12(1):31-42
Microbiota intestinal humana y dieta
vegetales; predominantemente vegetariana. Todos los
vida entre las 2 regiones; posiblemente fuente de agua
recursos alimenticios son completamente producidos
potable y uso de antibióticos (Mah et al., 2008).
localmente; granos de mijo, sorgo, leguminosas y otros
Se está investigando la relación entre la salud
vegetales, por lo que el contenido de carbohidratos, fibra
humana y taxones bacterianos comunes encontrados
y proteína vegetal es muy alto. A veces consumen una
en la microbiota humana. Enfermedades crónicas
pequeña cantidad de pollo y termitas en temporada de
como la obesidad, enfermedad inflamatoria intestinal,
lluvias. Los niños son amamantados hasta la edad de 2
diabetes mellitus, síndrome metabólico, aterosclerosis,
años como complemento a una dieta mixta. La cantidad
enfermedad hepática alcohólica, cirrosis y el carcinoma
promedio de fibra en la dieta es 10.0 g/d en niños de 1
hepatocelular se han asociado con la microbiota humana
a 2 años y 14.2 g/d en niños de 2 a 6 años. La dieta de
(Wang et al., 2017). Las personas con exceso de peso
los niños italianos es alta en proteína animal, azúcar,
presentan diferencias en la microbiota con relación
almidón, grasa y baja en fibra. Los niños amamantados
a personas delgadas. La manipulación dietética de
hasta 1 año de edad. La cantidad promedio de fibra en la
la microbiota a través de estrategias que favorezcan el
dieta es 5.6 g/d en niños de 1 a 2 años y 8.4 g/d en niños
crecimiento de las bacterias “beneficiosas” frente a las
de 2 a 6 años. Diferencias relevantes se encontraron
descritas como “patógenas” se considera una alternativa
en los filos. Actinobacteria y Bacteroidetes estuvieron
potencial a la hora de tratar o prevenir el desarrollo de
más representados en la microbiota de los niños Mossi
diversas patologías como la obesidad (Etxeberria et al.,
que en la de los niños italianos con abundancia única
2016). Mayor abundancia de Akkermansia muciniphila
de bacterias del género Prevotella y Xylanibacter, que
se asocia con un estado metabólico más saludable en
se sabe contienen un conjunto de genes bacterianos
humanos con sobrepeso/obesos (Dao et al., 2016).
para la hidrólisis de celulosa y xilano; completamente
Los efectos del predominio o disminución
ausentes en los niños italianos. Shigella y Escherichia
de comunidades de distintos filos pueden ser
(Enterobacteriaceae) estuvieron significativamente
transgeneracionales. Y cabe destacar que, la
subrepresentadas en los niños Mossi. Los filos Firmicutes
biodiversidad medioambiental contribuye a dar forma a
y Proteobacteria fueron más abundantes en los niños
la microbiota humana y las diferencias en la abundancia
italianos. La distribución diferencial de Firmicutes y
y diversidad bacterianas están asociadas con la salud.
Bacteroidetes marcó las profundas diferencias entre los
En consecuencia, cambios en la comunidad microbiana
2 grupos.
medioambiental en áreas contaminadas pueden llevar a
La acumulación de datos sugiere que, entre las
efectos similares en la comunidad microbiana humana y
poblaciones occidentales, Bacteroides se asocia
las consiguientes consecuencias para la salud (Parajuli
con dietas basadas en carne, Ruminococcaceae y
et al.,
2017). Además, diferencias en las estructuras
Lachnospiraceae con dietas ricas en polisacáridos
sociales pueden influir en el alcance de la transmisión
complejos de plantas y Prevotella con dietas altas en
de la microbiota y el flujo de microbios y genes
azúcar pero bajas en grasas y proteínas (Korpela, 2018).
microbianos entre miembros de un hogar. Diferencias
Efectos bifidogénicos se han observado en adultos
en las tradiciones culturales también afectan al alimento,
que consumieron manzanas (Shinohara et al., 2010) y
la exposición a mascotas y ganado, y muchos otros
bananas (Mitsou et al., 2011). La jalea de hipocolitos de
factores que podrían influir en cómo y desde dónde
maca (Lepidium meyenii) ejerció un efecto bifidogénico
una microbiota intestinal/microbioma se adquiere
cuando se incorporó a yogur, por incrementos en los
(Yatsunenko et al., 2012).
recuentos de Bifidobacterium bifidum (León-Marroú,
2011).
Se han observado disminuciones en la abundancia
Química de la dieta y microbiota intestinal
del grupo Clostridium en estudios que complementan el
La microbiota intestinal ejerce importantes
afrecho de arroz, garbanzos, manzanas, hongos, y frutas
actividades metabólicas mediante la extracción de
y otros vegetales bajos en contenidos de flavonoides
energía en polisacáridos de la dieta que de otra forma
(Sheflin et al., 2017).
no serían digeribles, como el almidón resistente y las
En la microbiota intestinal, niveles más altos de
fibras dietéticas. Estas actividades metabólicas también
bacterias ácido lácticas, coliformes y estafilococos,
conducen a la producción de nutrientes importantes,
y ninguna diferencia en enterococos, se encontraron
como los ácidos grasos de cadena corta
(AGCC),
en niños que viven en zona rural de Tailandia en
vitaminas
(p. ej., vitamina K, vitamina B12, ácido
comparación con zona urbana en Singapur. Las
fólico) y aminoácidos, que los humanos no pueden
diferencias pueden ser explicadas por el contraste de
producir por sí mismos (Gerritsen et al., 2011).
los factores medioambientales y prácticas de estilo de
Las proteínas, grasas y carbohidratos son los
Ciencia y Tecnología. 2019. 12(1):31-42
35
Padrón, 2019
principales componentes en las dietas de los humanos.
bacterias comensales Bifidobacterium y Lactobacillus,
El tipo y la cantidad de proteínas, grasas y carbohidratos
y adicionalmente el suero lácteo disminuye a las
presentes en la dieta influyen en la composición de la
bacterias patógenas Bacteroides fragilis y Clostridium
microbiota intestinal en el huésped. Este efecto está
perfringens
(Świątecka et al.,
2011; Singh et al.,
relacionado con los metabolitos de los componentes
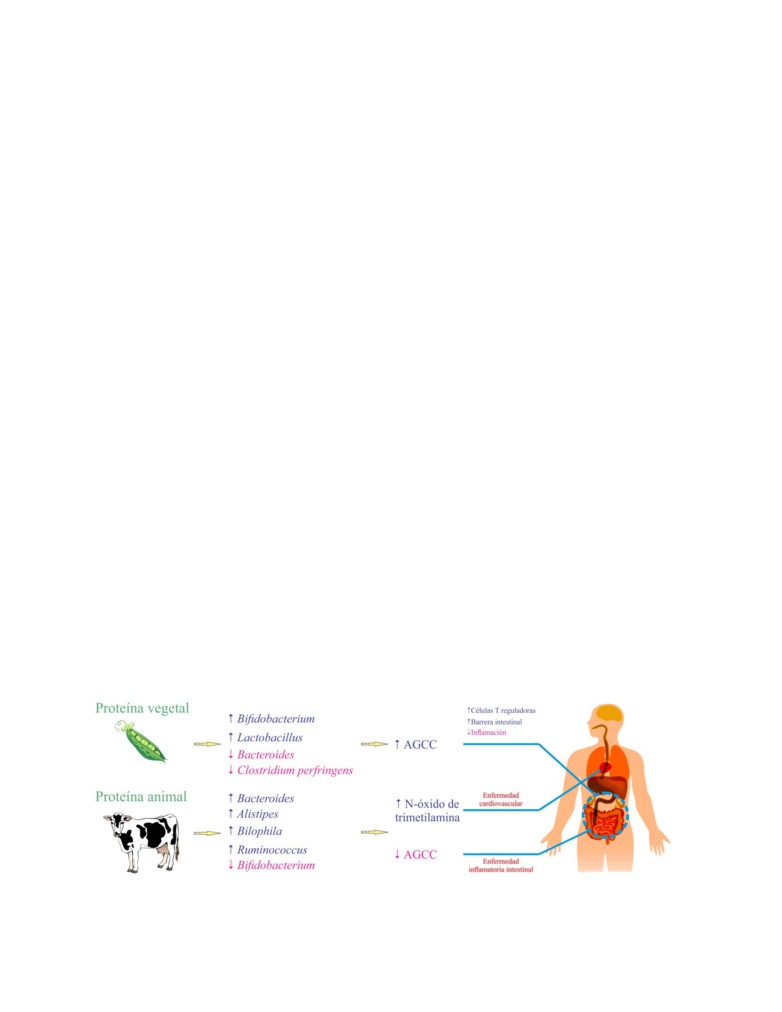
2017). Por el contrario, anaerobios como Alistipes,
presentes en las dietas. Los AGCC, predominantemente
Bilophila wadsworthia y Bacteroides se incrementan
acetato, propionato y butirato, son productos finales
con el consumo de dietas basadas en animales
de la degradación de proteínas y carbohidratos en el
(Figura 3); Alistipes putredinis y Bacteroides spp. son
tracto gastrointestinal, mediada por microorganismos.
microorganismos putrefactivos (David et al.,
2014).
Los AGCC producidos por la microbiota son los
Varios géneros microbianos promovidos por la ingesta
metabolitos más extensamente estudiados de las dietas
de una dieta omnívora se han asociado con incremento
y ha sido encontrado que tienen un efecto fisiológico
en los niveles del N-óxido de trimetilamina; compuesto
en la salud del huésped (Macfarlane y Macfarlane,
proaterogénico que aumenta el riesgo de enfermedad
2012; Rajoka et al., 2017). Las concentraciones de
cardiovascular (De Filippis et al., 2016). Las proteínas
todos los AGCC son típicamente más altas en el colon
derivadas de plantas se asocian con una menor
proximal (primera parte y parte media del intestino
mortalidad que las proteínas derivadas de animales
grueso) donde la fermentación es mayor y la cantidad
(Levine et al., 2014).
presente se relaciona con el suministro de carbohidratos
La grasa de la dieta normalmente es absorbida en el
en la dieta. En humanos, la abundancia de AGCC es
intestino delgado, y solo pequeñas cantidades alcanzan
típicamente acetato > propionato > butirato (Lockyer y
el intestino grueso. La grasa no es una fuente de energía
Nugent, 2017). En relación con el trabajo de De Filippo
primaria para la microbiota colónica (Korpela, 2018).
et al. (2010), se encontraron más AGCC en los niños
El consumo de una dieta baja en grasas condujo
Mossi que en los niños italianos; y en el de Schnorr et
a una mayor abundancia de Bifidobacterium con
al. (2014), los italianos se caracterizaron por una mayor
reducciones concomitantes en glucosa y colesterol
abundancia de butirato, mientras que los Hadza en
total, en comparación con el valor inicial. Por otro
propionato. Estas diferencias reflejaron la variación de
lado, una dieta alta en grasas saturadas aumentó la
la dieta en la cantidad y el tipo de fibra y carbohidratos
proporción relativa de Faecalibacterium prausnitzii; y
consumidos por ambos grupos.
sujetos con ingesta alta de grasas monoinsaturadas no
Entre los patrones dietéticos, alto consumo de
experimentaron cambios en la abundancia relativa de
carbohidratos complejos se asocia con Prevotella,
cualquier género bacteriano (Fava et al., 2013; Singh et
mientras que alto consumo de grasa/proteína con
al., 2017). Existe un creciente interés en F. prausnitzii,
Bacteroides. (Wu et al., 2011). En general, resultados
una de las especies bacterianas más abundantes que se
indican que Bacteroides, junto con Alistipes y
encuentran en el intestino, dado su papel potencialmente
Parabacteroides, puede ser el taxón proteolítico
importante en la promoción de la salud intestinal (Lopez-
primario en el intestino grueso de humanos (Korpela,
Siles et al., 2017). El consumo de dietas altas en grasas
2018).
saturadas y trans aumenta el riesgo de enfermedades
El consumo de suero lácteo y extracto proteínico
cardiovasculares a través de la regulación al alza del
de guisantes verdes (Pisum sativum) incrementa a las
colesterol total y lipoproteínas de baja densidad (‘low
Figura 3. Impacto de la proteína dietética en la microbiota intestinal y resultados de salud. Modificado de
Singh et al. (2017).
36
Ciencia y Tecnología. 2019. 12(1):31-42
Microbiota intestinal humana y dieta
density lipoproteins’, LDL) en la sangre. Las dietas
bohidratos no digeribles, como la cebada de grano ente-
ricas en grasa interactúan de diversas maneras con la
ro, resulta en enriquecimiento de los géneros Roseburia,
microbiota intestinal para facilitar la translocación de
Bifidobacterium, Dialister y las especies Eubacterium
los lipopolisacáridos bacterianos que contribuyen a la
rectale, Roseburia faecis y Roseburia intestinalis (Keim
generación de inflamación crónica (Sheflin et al., 2017).
y Martin, 2014); y el almidón resistente incrementa a
Por otro lado, las grasas promotoras de la salud, como las
Ruminococcus bromii y Eubacterium rectal (Walker et
grasas monoinsaturadas y poliinsaturadas, son cruciales
al., 2011; Sheflin et al., 2017). Versiones integrales de
para aliviar el riesgo de enfermedades crónicas. La dieta
alimentos con almidón (p. ej., pasta de trigo integral,
occidental típica es alta en grasas saturadas, trans y baja
arroz integral) contienen más almidón resistente que
en grasas monoinsaturadas, poliinsaturadas, por lo que
las versiones refinadas (Lockyer y Nugent, 2017). Los
predispone a los consumidores habituales a muchos
carbohidratos no digeribles pueden producir marcados
problemas de salud (Singh et al., 2017).
cambios en la microbiota intestinal, pero son depen-
Los carbohidratos digeribles se degradan
dientes de la composición inicial de la microbiota in-
enzimáticamente en el intestino delgado e incluyen
testinal individual (Walker et al., 2011). El consumo de
almidones y azúcares. Tras la degradación, estos
granos enteros y carbohidratos complejos no digeribles
compuestos liberan glucosa en el torrente sanguíneo
encontrados en granos integrales puede cambiar signifi-
y estimulan una respuesta a la insulina. Los humanos
cativamente la ecología microbiana del intestino grueso
alimentados con altos niveles de glucosa, fructosa y
(Keim y Martin, 2014). Cabe destacar que, R. bromii es
sacarosa, en forma de frutas de estación o temporada,
una especie clave que inicia la degradación del almidón
aumentan la abundancia relativa de Bifidobacterium y
resistente y produce subproductos que son más fácil-
reducen Bacteroides (Singh et al., 2017).
mente utilizados por otras especies intestinales (Sheflin
A diferencia de los carbohidratos digeribles, los car-
et al., 2017); y en el mismo sentido, bifidobacterias y
bohidratos no digeribles como la fibra y el almidón re-
lactobacilos metabolizan fructanos para producir lactato
sistente no se degradan enzimáticamente en el intestino
y acetato, como productos finales, que luego son utili-
delgado, sino que llegan al intestino grueso donde se
zados por muchas otras bacterias, incluidas Roseburia,
someten a la fermentación por parte de los microorga-
Eubacterium y Faecalibacterium, que producen butira-
nismos residentes produciendo AGCC (Lockyer y Nu-
to (Holscher, 2017).
gent, 2017). En consecuencia, la fibra dietética es buena
Entre los efectos de dietas muy bajas en carbohidratos,
fuente de “carbohidratos accesibles a la microbiota”,
en la microbiota intestinal ocurre disminución en
que pueden ser utilizados por los microorganismos para
la abundancia de bacterias productoras de butirato
proporcionar al huésped energía y fuente de carbono.
(Roseburia, Eubacterium rectale, Bifidobacterium), y
En el proceso, pueden modificar el entorno intestinal.
por ende, de butirato. El aumento de la ingesta de fibra
Esta propiedad de las fibras garantiza su designación
dietética no ha demostrado tener un efecto bifidogénico,
como prebióticos, que por definición son componen-
pero se ha asociado con un aumento en la riqueza y/o
tes dietéticos no digeribles que benefician la salud del
diversidad microbiana intestinal, especialmente en
huésped a través de la estimulación selectiva del creci-
individuos con una diversidad reducida inicialmente
miento y/o la actividad de ciertos microorganismos. Las
(Sheflin et al., 2017). Existe evidencia de que el almidón
fuentes de prebióticos incluyen la soya, inulinas, trigo
resistente puede contrarrestar los efectos perjudiciales
y cebada sin refinar, avena cruda y oligosacáridos no
de la alta ingesta de carne roja en el riesgo de cáncer
digeribles como los fructanos, polidextrosa, fructooli-
colorrectal (Lockyer y Nugent, 2017). Después de un
gosacáridos, galactooligosacáridos, xilololosacáridos y
alto consumo de carne y en ausencia de carbohidratos
arabinooligosacáridos (Singh et al., 2017). El consumo
fermentables, la carne roja puede producir aductos de
de cereales de maíz integral aumenta a Bifidobacterium
ADN promutagénicos y alterar la composición de la
spp. y Atobium spp., y el de trigo integral, la abundancia
microbiota. Por lo tanto, una dieta alta en proteínas
de lactobacilos y enterococos, además de Bifidobacte-
y baja en carbohidratos puede alterar la microbiota
rium spp. (Sheflin et al., 2017). Las dietas de carbohi-
colónica favoreciendo un perfil de microbiota más
dratos no digeribles que son ricas en grano integral y
proinflamatoria y una menor producción de AGCC.
afrecho de trigo están relacionadas con un aumento en
El consumo en conjunto con carbohidrato fermentable
el intestino de bifidobacterias y lactobacilos (Costabile
puede reducir este efecto, el almidón resistente previene
et al., 2008); este efecto prebiótico sobre bifidobacterias
la formación de aductos inducidos por la carne roja;
también ha sido observado con grano integral de maíz,
esto asociado con el aumento de los niveles de AGCC
lo que resultó en un cambio beneficioso en la microbiota
y cambios en la composición de la microbiota (Le Leu
(Carvalho-Wells et al., 2010). El consumo de otros car-
et al., 2015).
Ciencia y Tecnología. 2019. 12(1):31-42
37
Padrón, 2019
Identificar los efectos de la fibra dietética en la
totales y especies beneficiosas de Bifidobacterium y
microbiota intestinal se complica por diferencias en las
Eubacterium. El consumo de una dieta occidental se ha
estructuras químicas, otros componentes de los alimentos,
asociado con la producción de nitrosaminas promotoras
la variación del huésped y las metodologías de estudio.
del cáncer (Singh et al., 2017). La dieta mediterránea
No obstante, algunos patrones similares son aumentos
es considerada como una dieta sana y equilibrada. Se
frecuentes en Bifidobacterium spp., Ruminococcus
distingue por un perfil de ácidos grasos beneficiosos rico
spp., Eubacterium spp. y Faecalibacterium prausnitzii
en ácidos grasos monoinsaturados y poliinsaturados,
(Sheflin et al., 2017).
altos niveles de polifenoles y otros antioxidantes, alta
La fermentabilidad de las celulosas dietéticas en
ingesta de fibra y otros carbohidratos de bajo índice
el intestino humano varía según la fuente de alimento
glucémico, y relativamente mayor ingesta de proteínas
y la composición bacteriana intestinal. Las bacterias
vegetales que de origen animal. Específicamente, aceite
intestinales que degradan la celulosa se pueden
de oliva, frutas, cereales, nueces y otros vegetales;
dividir en productoras de metano, predominantemente
consumo moderado de pescado, carne de aves, y una
Bacteroidetes, y no productoras de metano,
menor ingesta de productos lácteos, carne roja, carne
predominantemente Firmicutes. Las especies que
procesada y dulces caracterizan a la dieta mediterránea
degradan la celulosa durante la digestión dependen
tradicional (Lopez-Legarrea et al., 2014). De Filippis et
de la estructura específica de la celulosa que se está
al. (2016) investigaron los beneficios potenciales de la
consumiendo y pueden incluir Clostridium spp.,
dieta mediterránea comparando omnívoros, vegetarianos
Eubacterium spp., Ruminococcus spp. y Bacteroides
y veganos. Observaron que la mayoría de los vegetarianos
spp. Tanto la celulosa como la hemicelulosa son
y veganos, pero solo el 30 % de los omnívoros, tenían
componentes mayoritarios de las paredes celulares
una alta adherencia a la dieta mediterránea. Detectaron
de las plantas y las hemicelulosas pueden dividirse
asociaciones significativas entre el grado de adherencia
en
arabinoxilanos,
xiloglucanos,
β-glucanos,
a la dieta mediterránea y el aumento de los niveles de
glucomananos y galactomananos. El tamaño molecular
AGCC fecales, bacterias Prevotella y otros Firmicutes.
de las hemicelulosas juega un papel en sus efectos sobre
A su vez, la baja adherencia a la dieta mediterránea se
la comunidad bacteriana intestinal (Sheflin et al., 2017).
asoció con N-óxido de trimetilamina urinario elevado,
Antes se creía que no era necesario incluir la fibra en la
que se asocia con riesgo de ateroesclerosis y desórdenes
dieta (salvo por garantía para prevenir el estreñimiento)
cardiovasculares.
porque los humanos no producen enzimas para degradar
La enfermedad cardiovascular
representa
celulosa o hemicelulosa, pero bacterias en la microbiota
la principal causa de muerte y morbilidad en el
intestinal llevan a cabo esas funciones.
mundo. En la microbiota intestinal el metabolismo
Hasta ahora, los modelos animales se han utilizado
de la fosfatidilcolina, colina y L-carnitina produce
principalmente para investigar la influencia de las
trimetilamina, que luego es metabolizado a N-óxido
pectinas en la microbiota intestinal. En ratas, aumentó la
de trimetilamina. Los alimentos ricos en lípidos
abundancia de Bacteroides spp. con pectina de cítricos;
fosfatidilcolina, que incluyen predominantemente
y la de Anaeroplasma, Anaerostipes y Roseburia
huevos, leche, hígado, carnes rojas, aves de corral,
con pectina de manzana, que también disminuyó la
mariscos y pescados, se cree que son las principales
abundancia de Alistipes y Bacteroides spp. Estos
fuentes dietéticas de colina, y por lo tanto la producción
resultados sugieren que la estructura de las pectinas es
de N-óxido de trimetilamina (Wang et al., 2011). La
un determinante del efecto sobre la microbiota intestinal
L-carnitina es un nutriente abundante en carnes rojas
y varía con la fuente de alimento (Sheflin et al., 2017).
y contiene una estructura similar a la de la colina.
Se han estudiado varias dietas, incluidas la
Los humanos omnívoros producen más N-óxido de
occidental, libre de gluten, omnívora, vegetariana,
trimetilamina que los vegetarianos y veganos (Koeth
vegana y la mediterránea, por su capacidad para
et al., 2013).
modular la microbiota intestinal. Las dietas vegetariana
Otros estudios han demostrado que los alimentos
y vegana están enriquecidas con alimentos fermentables
que comprenden la dieta mediterránea típica ofrecen
a base de plantas. La dieta mediterránea es un marcado,
mejoría en relación con la obesidad, el perfil lipídico
pero no exclusivamente, estilo de dieta vegetariano, que
y la inflamación. Estos cambios pueden estar mediados
ha demostrado ser beneficioso para el tratamiento de la
por aumentos derivados de la dieta en Lactobacillus,
obesidad, la diabetes tipo 2, enfermedades inflamatorias
Bifidobacterium, Prevotella, y disminuciones en
y enfermedades cardiovasculares (De Filippis et al.,
Clostridium (Singh et al., 2017).
2016). En varios estudios, una dieta occidental (alta
La dieta puede modificar la microbiota intestinal,
en proteína y grasa animal, y baja en fibra) condujo a
lo que a su vez tiene un profundo impacto en la salud
una marcada disminución en el número de bacterias
general. Este impacto puede ser beneficioso o perjudicial,
38
Ciencia y Tecnología. 2019. 12(1):31-42
Microbiota intestinal humana y dieta
dependiendo de la identidad relativa y la abundancia de
bacterias viven en el intestino de los primates, lo que
poblaciones bacterianas constituyentes (Singh et al.,
contribuye al metabolismo, al desarrollo del sistema
2017). La microbiota intestinal, compuesta por billones
inmune y a la resistencia a patógenos. Las perturbaciones
de organismos comensales no patógenos, sirve como
de esas bacterias están asociadas con enfermedades
filtro para nuestra mayor exposición medioambiental, lo
humanas metabólicas y autoinmunes que prevalecen en
que comemos (Wang et al., 2011).
las sociedades occidentalizadas. Clayton et al. (2016)
A pesar de la relevancia evolutiva, pocos estudios
usaron la secuenciación de genes ARN ribosómico 16S
comparan sistemáticamente microbiomas intestinales
en modelos de 2 especies de primates no humanos.
de primates humanos y no humanos. La comparación
Midieron las comunidades microbianas intestinales y
directa de microbiomas de primates (humanos y no
la dieta en múltiples especies de primates que viven
humanos) ofrece información sobre qué factores
en estado salvaje, en un santuario y en completo
moldearon el microbioma a lo largo del pasado
cautiverio. Encontraron que el cautiverio y la pérdida
evolutivo. Los datos que existen demuestran que, en
de fibra dietética en primates no humanos estuvieron
contraste con ancestros comunes más recientes (simios
asociados con la pérdida de la microbiota intestinal
africanos), los humanos tienen una baja diversidad
nativa y la convergencia hacia el microbioma humano
de microbiota intestinal, mayor abundancia relativa
moderno, lo que sugirió, que procesos paralelos pueden
de Bacteroides y menor abundancia relativa de
estar impulsando la pérdida reciente de la biodiversidad
Methanobrevibacter y Fibrobacter. Muchos de estas
microbiana central en humanos.
características están asociadas con la carnivoría en
otros mamíferos, lo que sugiere que un cambio en la
Conclusiones
dieta humana hacia el consumo de carne en escalas
de tiempo evolutivas puede haber estado acompañado
La dieta modifica el microbioma intestinal y los efectos
por cambios microbianos intestinales asociados. La
beneficiosos o perjudiciales de las dietas están mediados
comparación de microbiomas de primates humanos y
por la microbiota y dependen de la identidad relativa y la
no humanos también proporciona una indicación de
abundancia de poblaciones bacterianas constituyentes.
qué tan rápido está cambiando el microbioma humano.
La composición de la microbiota depende del tipo y la
La composición del microbioma intestinal humano
disponibilidad de sustratos proporcionados en la dieta
parece haber divergido del estado ancestral a un ritmo
habitual. Dietas basadas en plantas y animales tienen
acelerado en comparación con la de los grandes simios.
efectos diferentes sobre la ecología de la microbiota
Algunas de las características de la evolución humana
intestinal y sus productos metabólicos. Una microbiota
y la historia potencialmente responsable incluyen los
favorable produce resultados en beneficio de la salud
alimentos cocidos, el advenimiento de la agricultura,
del huésped y se logra con dietas ricas en carbohidratos
el tamaño de la población y los aumentos de densidad
y bajas en proteínas/grasas. La dieta puede usarse
(Davenport et al., 2017).
para modular la composición y el metabolismo de la
La asociación entre la dieta y la relación de
microbiota intestinal.
parentesco
(filogenia) en microbiomas de primates
se hace eco de patrones más amplios de diversidad
Bibliografía
entre las comunidades intestinales de vertebrados.
Las transiciones a herbivoría parecen tener efectos
Biagi, E., Franceschi, C., Rampelli, S., Severgnini, M., Ostan,
especialmente grandes en el microbioma. Los mamíferos
R., Turroni, S., Consolandi, C., Quercia, S., et al. 2016.
con dietas herbívoras de evolución independiente
Gut microbiota and extreme longevity. Current Biology.
albergan una microbiota similar. Además, algunos de
26(11):1480-1485.
los mismos genes y rutas que difieren en abundancia
Bian, G., Gloor, G.B., Gong, A.. Jia, Ch., Zhang, W., Hu, J.,
entre los microbiomas herbívoros y carnívoros, también
Zhang, H., Zhang, Y., et al. 2017. The gut microbiota
cambian rápidamente en direcciones correspondientes
of healthy aged Chinese is similar to that of the healthy
en seres humanos que cambian de dietas vegetarianas a
young. mSphere. 2(5):e00327-17. 12 p.
las omnívoras (Davenport et al., 2017).
Carvalho-Wells, A.L., Helmolz, K., Nodet, C., Molzer, C.,
El ARN ribosómico
16S es la macromolécula
Leonard, C., McKevith, B., Thielecke, F., Jackson,
más ampliamente utilizada en estudios de filogenia y
K.G., et al. 2010. Determination of the in vivo prebiotic
taxonomía bacterianas para establecer las relaciones
potential of a maize-based whole grain breakfast cereal:
filogenéticas dentro del mundo procariota, causando
a human feeding study. British Journal of Nutrition.
un profundo impacto en la visión de la evolución y,
104(9):1353-1356.
como consecuencia, en la clasificación e identificación
Chen, T., Kim, Ch.Y., Kaur, A., Lamothe, L., Shaikh, M.,
bacteriana
(Rodicio y Mendoza, 2004). Billones de
Keshavarzian, A. and Hamaker, B.R. 2017. Dietary
Ciencia y Tecnología. 2019. 12(1):31-42
39
Padrón, 2019
fibre-based SCFA mixtures promote both protection and
37:216-223.
repair of intestinal epithelial barrier function in a Caco-2
Flint, H.J., Scott, K.P., Louis, P. and Duncan, S.H. 2012. The
cell model. Food & Function. 8(3):1166-1173.
role of the gut microbiota in nutrition and health. Nature
Claesson, M.J., Jeffery, I.B., Conde, S., Power, S.E.,
Reviews Gastroenterology & Hepatology. 9:577-589.
O’Connor, E.M., Cusack, S., Harris, H.M.B., Coakley,
Fukuda, S., Toh, H., Hase, K., Oshima, K., Nakanishi, Y.,
M., et al. 2012. Gut microbiota composition correlates
Yoshimura, K., Tobe, T., Clarke, J.M., et al. 2011.
with diet and health in the elderly. Nature. 488:178-184.
Bifidobacteria can protect from enteropathogenic
Clayton, J.B., Vangay, P., Huang, H., Ward, T., Hillmann,
infection through production of acetate. Nature.
B.M., Al-Ghalith, G.A., Travis, D.A., Long, H.T., et
469:543-547.
al. 2016. Captivity humanizes the primate microbiome.
Gerritsen, J., Smidt, H., Rijkers, G.T. and de Vos, W.M. 2011.
Proceedings of the National Academy of Sciences
Intestinal microbiota in human health and disease: the
(USA). 13(37):10376-10381.
impact of probiotics. Genes & Nutrition. 6(229):209-
Costabile, A., Klinder, A., Fava, F., Napolitano, A., Fogliano,
240.
V., Leonard, C., Gibson, G.R. and Tuohy, K.M. 2008.
Gibson, G.R., Hutkins, R., Sanders, M.E., Prescott, S.L.,
Whole-grain wheat breakfast cereal has a prebiotic effect
Reimer, R.A., Salminen, S.J., Scott, K., Stanton, C., et
on the human gut microbiota: a double-blind, placebo-
al. 2017. Expert consensus document: The International
controlled, crossover study. British Journal of Nutrition.
Scientific Association for Probiotics and Prebiotics
99(1):110-120.
(ISAPP) consensus statement on the definition and
D’Argenio, V. and Salvatore, F. 2015. The role of the gut
scope of prebiotics. Nature Reviews Gastroenterology
microbiome in the healthy adult status. Clinica Chimica
& Hepatology. 14:491-502.
Acta. 45(Part A):97-102.
Graf, D., Di Cagno, R., Fak, F., Flint, H.J., Nyman, M.,
Dao, M.C., Everard, A., Aron-Wisnewsky, J., Sokolovska,
Saarela, M. and Watz, B. 2015. Contribution of diet to
N., Prifti, E., Verger, E.O., Kayser, B.D., Levenez, F.,
the composition of the human gut microbiota. Microbial
et al.
2016. Akkermansia muciniphila and improved
Ecology in Health and Disease. 26(1):26164. 11 p.
metabolic health during a dietary intervention in obesity:
Hehemann, J.H., Correc, G., Barbeyron, T., Helbert,
relationship with gut microbiome richness and ecology.
W., Czjzek, M. and Michel, G.
2010. Transfer of
Gut. 65(3):426-436.
carbohydrate-active enzymes from marine bacteria to
Davenport, E.R., Sanders, J.G., Song, S.J., Amato, K.R., Clark,
Japanese gut microbiota. Nature. 464:908-912.
A.G. and Knight, R. 2017. The human microbiome in
Hill, C., Guarner, F., Reid, G., Gibson, G.R., Merenstein,
evolution. BMC Biology. 15:127. 12 p.
D.J., Pot, B., Morelli, L., Canani, R.B., et al. 2014.
De Filippis, F., Pellegrini, N., Vannini, L., Jeffery, I.B., La
The International Scientific Association for Probiotics
Storia, A., Laghi, L., Serrazanetti, D.I., Di Cagno, R., et
and Prebiotics consensus statement on the scope and
al. 2016. High-level adherence to a Mediterranean diet
appropriate use of the term probiotic. Nature Reviews
beneficially impacts the gut microbiota and associated
Gastroenterology & Hepatology. 11:506-514.
metabolome. Gut. 65(11):1812-1821.
Holscher, H.D. 2017. Dietary fiber and prebiotics and the
De Filippo, C., Cavalieri, D., Di Paola, M., Ramazzotti, M.,
gastrointestinal microbiota. Gut Microbes.
8(2):172-
Poullet, J.B., Massart, S., Collini, S., Pieraccini, G., et al.
184.
2010. Impact of diet in shaping gut microbiota revealed
Hugon, P., Dufour, J.Ch., Colson, P., Fournier, P.E., Sallah,
by a comparative study in children from Europe and
K. and Raoult, D. 2015. A comprehensive repertoire
rural Africa. Proceedings of the National Academy of
of prokaryotic species identified in human beings. The
Sciences. 107(33):14691-14696.
Lancet Infectious Diseases. 15(10):1211-1219.
David, L.A., Maurice, C.F., Carmody, R.N., Gootenberg, D.B.,
Keim, N.L. and Martin, R.J. 2014. Dietary whole grain-
Button, J.E., Wolfe, B.E., Ling, A.V., Devlin, A.S., et al.
microbiota interactions: insights into mechanisms for
2014. Diet rapidly and reproducibly alters the human gut
human health. Advances in Nutrition. 5:556-557.
microbiome. Nature. 505:559-563.
Kiefer, J., Beyer-Sehlmeyer, G. and Pool-Zobel, B.L.
Etxeberria, U., Milagro, F.I., González-Navarro, C.J.
2006. Mixtures of SCFA, composed according to
y Martínez, J.A. 2016. Papel en la obesidad de la
physiologically available concentrations in the gut
microbiota intestinal. Anales de la Real Academia
lumen, modulate histone acetylation in human HT29
Nacional de Farmacia. 82:234-259.
colon cancer cells. British Journal of Nutrition.
Fava, F., Gitau, R., Griffin, B.A., Gibson, G.R., Tuohy, K.M.
96(5):803-810.
and Lovegrove, J.A. 2013. The type and quantity of
Klemashevich, C., Wu, Ch., Howsmon, D., Alaniz, R.C., Lee,
dietary fat and carbohydrate alter faecal microbiome and
K. and Jayaraman, A. 2014. Rational identification
short-chain fatty acid excretion in a metabolic syndrome
of diet-derived postbiotics for improving
‘at-risk’ population. International Journal of Obesity.
intestinal microbiota function. 26:85-90.
40
Ciencia y Tecnología. 2019. 12(1):31-42
Microbiota intestinal humana y dieta
Koeth, R.A., Wang, Z., Levison, B.S., Buffa, J.A., Org, E.,
Muegge, B.D., Kuczynski, J., Knights, D., Clemente, J.C.,
Sheehy, B.T., Britt, E.B., Fu, X., et al. 2013. Intestinal
González, A., Fontana, L., Henrissat, B., Knight, R.
microbiota metabolism of L-carnitine, a nutrient in
and Gordon, J.I. 2011. Diet drives convergence in gut
red meat, promotes atherosclerosis. Nature Medicine.
microbiome functions across mammalian phylogeny
19:576-585.
and within humans. Science. 332(6032):970-974.
Korpela, K. 2018. Diet, microbiota, and metabolic health:
National Center for Complementary and Integrative Health
trade-off between saccharolytic and proteolytic
(NCCIH). 2018. Probiotics. U.S. Department of Health
fermentation. Annual Review of Food Science and
& Human Services, National, Institutes of Health.
Technology. 9:65-84.
Le Leu, R.K., Winter, J.M., Christophersen, C.T., Young,
Nishijima, S., Suda, W., Oshima, K., Kim, S.W., Hirose, Y.,
G.P., Humphreys, K.J., Hu, Y., Gratz, S.W., Miller, R.B.,
Morita, H. and Hattori, M. 2016. The gut microbiome
et al. 2015. Butyrylated starch intake can prevent red
of healthy Japanese and its microbial and functional
meat-induced O6-methyl-2-deoxyguanosine adducts in
uniqueness. DNA Research. 23(2):125-133.
human rectal tissue: a randomized clinical trial. British
Parajuli, A., Grönroos, M., Kauppi, S., Płociniczak, T.,
Journal of Nutrition. 114(2):220-230.
Roslund, M.I., Galitskaya, P., Laitinen, O.H., Hyöty, H.,
León-Marroú, M.E.
2011. Efecto bifidogénico de jalea
et al. 2017. The abundance of health-associated bacteria
de Lepidium meyenii Walp. “maca” en el recuento
is altered in PAH polluted soils-Implications for health
de Bifidobacterium bifidum en yogurt probiótico.
in urban areas? PLoS ONE. 12(11):e0187852.
Revista Venezolana de Ciencia y Tecnología de
Patel, S. and Goyal, A. 2012. The current trends and future
Alimentos. 2(1):094-107.
perspectives of prebiotics research: a review. 3 Biotech.
Levine; M.E., Suarez, J.A., Brandhorst, S., Balasubramanian,
2(2):115-125.
P., Cheng, C.W., Madia, F., Fontana, L., Mirisola, M.G.,
Rajoka, M.S.R., Shi, J., Mehwish, H.M., Zhu, J., Li, Q., Shao,
et al.
2014. Low protein intake is associated with a
D., Huang, Q. and Yang, H. 2017. Interaction between
major reduction in IGF-1, cancer, and overall mortality
diet composition and gut microbiota and its impact
in the 65 and younger but not older population. Cell
ongastrointestinal tract health. Food Science and Human
Metabolism. 19(3):407-417.
Wellness. 6(3):121-130.
Ley, R.E., Hamady, M., Lozupone, C., Turnbaugh, P.J.,
Rodicio, M. del R. y Mendoza, M del C. 2004. Identificación
Ramey, R.R., Bircher, J.S., Schlegel, M.L., Tucker,
bacteriana mediante secuenciación del ARNr
T.A., et al. 2008. Evolution of mammals and their gut
16S: fundamento, metodología y aplicaciones en
microbes. Science. 320(5883):1647-1651.
microbiología clínica. Enfermedades Infecciosas y
Lockyer, S. and Nugent, A.P. 2017. Health effects of resistant
Microbiología Clínica. 22(4):238-245.
starch. Nutrition Bulletin. 42(1):10-41.
Schnorr, S.L., Candela, M., Rampelli, S., Centanni, M.,
Lopez-Legarrea, P., Fuller, N.R., Zulet, M.A., Martinez, J.A.
Consolandi, C., Basaglia, G., Turroni, S., Biagi, E., et al.
and Caterson, ID. 2014. The influence of Mediterranean,
2014. Gut microbiome of the Hadza hunter-gatherers.
carbohydrate and high protein diets on gut microbiota
Nature Communications. 5:3654. 12 p.
composition in the treatment of obesity and associated
Sheflin, A.M., Melby, C.L., Carbonero, F. and Weir, T.L. 2017.
inflammatory state. Asia Pacific Journal of Clinical
Linking dietary patterns with gut microbial composition
Nutrition. 23(3):360-368.
and function. Gut Microbes. 8(2):113-129.
Lopez-Siles, M., Duncan, S.H., Garcia-Gil, L.J. and Martinez-
Shinohara, K., Ohashi, Y., Kawasumi, K., Terada, A. and
Medina, M. 2017. Faecalibacterium prausnitzii: from
Fujisawa, T.
2010. Effect of apple intake on fecal
microbiology to diagnostics and prognostics. The ISME
microbiota and metabolites in humans. Anaerobe.
Journal. 11:841-852.
16(5):510-515.
Macfarlane, G.T. and Macfarlane, S. 2012. Bacteria, colonic
Singh, R.K., Chang, H.W., Yan, D., Lee, K.M., Ucmak,
fermentation, and gas-trointestinal health. Journal of
D., Wong, K., Abrouk, M., Farahnik, B., et al. 2017.
AOAC International. 95(1):50-60.
Influence of diet on the gut microbiome and implications
Mah, K.W., Sangsupawanich, P., Tunyapanit, W., van Bever,
for human health. Journal of Translational Medicine.
H., Shek, L.P., Chua, K.Y. and Lee, B.W. 2008. Gut
15:73. 17 p.
microbiota of children living in rural south Thailand and
Slavin, J. 2013. Fiber and prebiotics: mechanisms and health
urban Singapore. Allergology International. 57(1):65-
benefits. Nutrients. 5(4):1417-1435.
71.
Świątecka, D., Narbad, A., Ridgway, K.P. and Kostyra, H.
Mitsou, E.K., Kougia, E., Nomikos, Tz., Yannakoulia, M.,
2011. The study on the impact of glycated pea proteins
Mountzouris, K.C. and Kyriacou, A. 2011. Effect of
on human intestinal bacteria. International Journal of
banana consumption on faecal microbiota: a randomised,
Food Microbiology. 145(1):267-272.
controlled trial. Anaerobe. 17(6):384-387.
Thursby, E. and Juge, N. 2017. Introduction to the human gut
Ciencia y Tecnología. 2019. 12(1):31-42
41
Padrón, 2019
microbiota. Biochemical Journal. 474(11):1823-1836.
Walker, A.W., Ince, J., Duncan, S.H., Webster, L.M., Holtrop,
G., Ze, X., Brown, D., Stares, M.D., et al. 2011. Dominant
and diet-responsive groups of bacteria within the human
colonic microbiota. The ISME Journal. 5:220-230.
Wang, B., Yao, M., Lv, L., Ling, Z. and Li, L. 2017. The
human microbiota in health and disease. Engineering.
3(1):71-82.
Wang, Z., Klipfell, E., Bennett, B.J., Koeth, R., Levinson,
B.S., DuGar, B., Feldstein, A.E., Britt, E.B., et al. 2011.
Gut flora metabolism of phosphatidylcholine promotes
cardiovascular disease. Nature. 472:57-63.
Wu, G.D., Chen, J., Hoffmann, Ch., Bittinger, K., Chen, Y.Y.,
Keilbaugh, S.A., Bewtra, M., Knights, D., et al. 2011.
Linking long-term dietary patterns with gut microbial
enterotypes. Science. 334(6052):105-108.
Yatsunenko, T., Rey, F.E., Manary, M.J., Trehan, I.,
Dominguez-Bello, M.G., Contreras, M., Magris, M.,
Hidalgo, G., et al. 2012. Human gut microbiome viewed
across age and geography. Nature. 486:222-227.
42
Ciencia y Tecnología. 2019. 12(1):31-42